Строение вещества
Около двух с половиной тысяч лет назад древнегреческий философ и исследователь природы Фалес Милетский впервые отмечает, что у гравитации есть могучий соперник, ранее ловко скрывавшийся от людей. Обнаружилось, что если натереть шерстью янтарную палочку, то палочка притягивает к себе легкие предметы, скажем клочки ткани.

Фалес Милетский (640 — 548 до н. э.)
Древнегреческий математик и философ
Представитель западной философии (Милетская школа).
Автор одноименной теоремы и календаря.
Последователи его идей Анаксшландр и Анаксимен.
Под действием своей тяжести, то есть под действием гравитационного притяжения к земле, эти клочки ткани должны были бы падать, двигаться вниз. А они, преодолевая силы гравитации, упрямо поднимаются вверх. Ответить на эти вопросы первые исследователи не могли, и лишь зафиксировали обнаруженный факт.
Дали новому явлению свое название-«электричество»
На русский язык это слово можно было бы перевести так: «янтарничество»
Потому, что «электричество» происходит от греческого слова «электрон», что означает «янтарь», и «электричеством» новое явление было названо именно потому, что оно было обнаружено в опытах с янтарной палочкой. Опыты с натиранием янтаря позволяют сделать очень важный вывод. До этих опытов было известно только одно основное свойство материи — масса, которая заставляла предметы притягиваться друг к другу, двигаться, работать. Натертый янтарь показал, что наряду с массой у вещества может быть еще одно работающее основное свойство, в дальнейшем ему дали название «электрический заряд». Почему электрический — понятно. Почему заряд? Трудно сказать...

Любопытно, что в английском языке в качестве слова «заряд» используют слово charg, имеющее много значений, в том числе «цена», «поручение», «обязанность», «атака». Так что там «электрический заряд» по смыслу, видимо, означает «электрическая цена», то есть мера электрических свойств.
Материя
Материей является все, что занимает окружающее нас пространство и имеет вес. Она бывает в одном из трех основных состояний: твердом, жидком или газообразном. Примерами материи являются: воздух, которым мы дышим, вода, которую пьем, одежда, которую носим, и мы сами. Материя может быть либо элементом, либо соединением. Элемент является основным строительным материалом природы. Он представляет собой субстанцию, которая не может быть разделена на более простые субстанции химическим путем. В настоящее время известно около 100 элементов. Примерами являются золото, серебро, медь и кислород. Химическая комбинация двух или более элементов называется соединением. Соединение может быть разделено химическим, но не механическим способом. Примерами соединений являются вода, которая состоит из кислорода и водорода. Поваренная соль, состоящая из натрия и хлора. Наименьшая частица соединения, которая еще сохраняет его свойства, называется молекулой. Молекула — это химическая комбинация двух или более атомов. Атом — это наименьшая частица элемента, сохраняющая характеристики элемента. Комбинация элементов и соединений, не вступивших в химическую реакцию, называется смесью. Примерами смесей являются воздух, состоящий из кислорода, азота, углекислого газа, и соленая вода, которая состоит из соли и воды.
Определение:
Химическая комбинация двух или более элементов называется соединением. Примером соединения явлется соленая вода = вода Н2О+ соль NaCl. Молекула — это химическая комбинация двух или более атомов.

1 и 2 атомы элементов.
Атом является наименьшей частицей элемента, сохраняющей его характеристики. Атомы различных элементов отличаются друг от друга. Поскольку существует свыше 100 различных элементов, то существует и свыше 100 различных видов атомов. Каждый атом имеет ядро. Ядро расположено в центре атома. Оно содержит положительно заряженные частицы (протоны) и незаряженные частицы (нейтроны). Отрицательно заряженные частицы (электроны) вращаются вокруг ядер. Сравнительно недавно, в середине семидесятых годов, начала активно развиваться и получать экспериментальное подтверждение физическая теория, согласно которой такие частицы, как протон и нейтрон (к электрону это не относится), состоят из еще более «мелких деталей» — кварков.

У кварков электрический заряд меньше, чем у протона, и может составлять '/з или 2/з от той порции электричества, которую имеет протон. Причем заряд кварков может быть как положительным, так и отрицательным. Однако теория предсказывает, что сами кварки выделить из протонов или других частиц и получить в «чистом виде» невозможно, а может быть, даже принципиально невозможно. Каждый элемент имеет атомный вес. Атомный вес — это масса атома, которая определяется общим числом протонов и нейтронов в ядре. Электроны практически не дают вклада в общую массу атома, масса электрона составляет только 1/1845 часть массы протона и ею можно пренебречь. Электроны вращаются по концентрическим орбитам вокруг ядра. Каждая орбита называется оболочкой. Эти оболочки заполняются в следующей последовательности: сначала заполняется оболочка К, затем L, М, N и т.д.

Одна из правдоподобных моделей атома похожа на нашу Солнечную систему, и ее так и называют — «планетарная модель». В центре планетарной модели — основная деталь атома, его ядро, массивный шар, в котором сосредоточена почти вся атомная масса. Вокруг ядра вращаются маленькие и легкие шарики — электроны, чем-то напоминая планеты, вращающиеся вокруг Солнца но, конечно же, планетарная модель — это упрощение, искажение истины. Скажем, электроны — это совсем не шарики-пылинки, а некоторые во многом еще загадочные сгустки материи, которые ведут себя не только как частицы, но и как волны. Внешняя оболочка называется валентной. Количество электронов, содержащееся в ней, называется валентностью. Чем дальше от ядра валентная оболочка, тем меньшее притяжение со стороны ядра испытывает каждый валентный электрон.

Таким образом, потенциальная возможность атома присоединять или терять электроны увеличивается, если валентная оболочка не заполнена и расположена достаточно далеко от ядра. Электроны валентной оболочки могут получать энергию. Если эти электроны получат достаточно энергии от внешних сил, они могут покинуть атом и стать свободными электронами, произвольно перемещающимися от атома к атому. Материалы, содержащие большое количество свободных электронов называются проводниками. На рисунке сравниваются проводимости различных металлов, используемых в качестве проводников. В таблице серебро, медь и золото имеют валентность равную единице. Однако серебро является лучшим проводником, поскольку его валентные электроны слабее связаны.

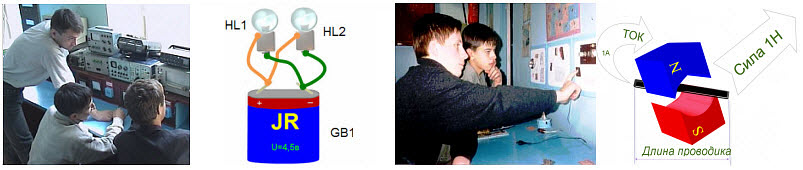
Изоляторы, в противоположность проводникам, препятствуют протеканию электричества. Изоляторы стабильны благодаря тому, что валентные электроны одних атомов присоединяются к другим атомам, заполняя их валентные оболочки, препятствуя, таким образом, образованию свободных электронов. Слюда является наилучшим изолятором, потому что она имеет наименьшее число свободных электронов на своих валентных оболочках. Промежуточное положение между проводниками и изоляторами занимают полупроводники.
Полупроводники не являются ни хорошими проводниками, ни хорошими изоляторами, но они важны, потому что их проводимость можно изменять от проводника до изолятора. Кремний и германий являются полупроводниковыми материалами. Об атоме, который имеет одинаковое число электронов и протонов, говорят, что он электрически нейтрален. Атом, получающий один или более электронов, не является электрически нейтральным. Он становится отрицательно заряженным и называется отрицательным ионом. Если атом теряет один или более электронов, то он становится положительно заряженным и называется положительным ионом. Процесс присоединения или потери электронов называется ионизацией. Ионизация играет большую роль в протекании электрического тока.

Группа шведских ученых из университета Лунда впервые засняла электрон, создав для этого квантовый стробоскоп, испускающий очень короткие лазерные вспышки. На записи можно видеть не движение точки в пространстве, а распределение энергии электрона как функцию от временной задержки ультрафиолетовой лазерной вспышки относительно колебания инфракрасного лазерного поля. То есть, каждый кадр – это распределение энергии электрона в данный момент времени.
Неужели электрон ?
Для управления движением электронов использовалось осциллирующее поле инфракрасного лазера. Поле временно ионизировало атомы гелия, то есть выбивало из них электроны, которые затем фиксировались детектором. Для получения более четкой картины, позволяющей наблюдать за поведением электронов во времени, использовались сверхкороткие ультрафиолетовые лазерные вспышки длительностью не более 300 аттосекунд (аттосекунда – 10 в -18 степени секунды), синхронизированные с колебаниями поля. Исследователи сравнивают этот метод с работой стробоскопа – прибора, который позволяет наблюдать быстрые периодические движения и получать их изображения, испуская быстро повторяющиеся короткие вспышки света.